Прежде чем мы описать систему MOVEOUT, я хочу, чтобы вы вообще понимали какие процессы происходят в мышцах при работе. Я не буду вдаваться в мельчайшие подробности, дабы не травмировать вашу психику, поэтому расскажу о самом важном. Что же, возможно многие не поймут этот раздел, но советую его хорошо изучить, так как благодаря нему вы поймете как работают наши мышцы, а значит поймете как их правильно тренировать.
Итак, основное, что нужно для работы наших мышц – это молекулы АТФ с которой мышцы получают энергию. От расщепления АТФ образуется молекула АДФ + энергия. Вот только запасов АТФ хватает в наших мышцах всего на 2 секунды работы, а далее идет ресинтез АТФ из молекул АДФ. Собственно, от типов процессов ресинтеза АТФ и зависит работоспособность и функциональность.
Итак, выделяют такие процессы. Они обычно подключаются друг за другом
1. Анаэробный креатинфосфатный
Главным преимуществом креатинфосфатного пути образования АТФ являются
- малой время развертывания,
- высокая мощность.

Креатинфосфатный путь связан с веществом креатинфосфатом . Креатинфосфат состоит из вещества креатина. Креатинфосфат обладает большим запасом энергии и высоким сродством с АДФ. Поэтому он легко вступает во взаимодействие с молекулами АДФ, появляющимися в мышечных клетках при физической работе в результате реакции гидролиза АТФ. В ходе этой реакции остаток фосфорной кислоты с запасом энергии переносится с креатинфосфата на молекулу АДФ с образованием креатина и АТФ.
Креатинфосфат + АДФ → креатин + АТФ.
Эта реакция катализируется ферментом креатинкиназой . Данный путь ресинтеза АТФ иногда называют креатикиназным, иногда фосфатным или алактатным.
Креатинфосфат – вещество непрочное. Образование из него креатина происходит без участия ферментов. Не используемый организмом креатин, выводится из организма с мочой. Синтез креатинфосфата происходит во время отдыха из избытка АТФ. При мышечной работе умеренной мощности запасы креатинфосфата могут частично восстанавливаться. Запасы АТФ и креатинфосфата в мышцах называют также фосфагены.
Фосфатная система отличается очень быстрым ресинтезом АТФ из АДФ, однако она эффективна только в течение очень короткого времени. При максимальной нагрузке фосфатная система истощается в течение 10 с. Вначале в течение 2 с расходуется АТФ, а затем в течение 6-8 с - КФ.
Фосфатная система называется анаэробной, потому что в ресинтезе АТФ не участвует кислород, и алактатной, поскольку не образуется молочная кислота.
Эта реакция является главным источником энергии для упражнений максимальной мощности: бег на короткие дистанции, прыжки метания, подъем штанги. Эта реакция может неоднократно включаться во время выполнения физических упражнений, что делает возможным быстрое повышение мощности выполняемой работы.
2. Анаэробный гликолиз

По мере увеличения интенсивности нагрузки наступает период, когда мышечная работа уже не может поддерживаться за счет одной только анаэробной системы из-за нехватки кислорода. С этого момента в энергообеспечение физической работы вовлекается лактатный механизм ресинтеза АТФ, побочным продуктом которого является молочная кислота. При недостатке кислорода молочная кислота, образовавшаяся в первой фазе анаэробной реакции, не нейтрализуется полностью во второй фазе, в результате чего происходит ее накопление в работающих мышцах, что приводит к ацидозу, или закислению, мышц.
Гликолитический путь ресинтеза АТФ, так же как креатинфосфатный является анаэробным путем. Источником энергии, необходимой для ресинтеза АТФ в данном случае является мышечный гликоген. При анаэробном распаде гликогена от его молекулы под действием фермента фосфорилазы поочередно отщепляются концевые остатки глюкозы в форме глюкозо-1-фосфата. Далее молекулы глюезо-1-фосфата после ряда последовательных реакций превращаются в молочную кислоту. Этот процесс называется гликолиз. В результате гликолиза образуются промежуточные продукты, содержащие фосфатные группы, соединенные макроэргическими связями. Эта связь легко переносится на АДФ с образованием АТФ. В покое реакции гликолиза протекают медленно, но при мышечной работе его скорость может возрасти в 2000 раз, причем уже в предстартовом состоянии.
Время развертывания 20-30 секунд.
Время работы с максимальной мощностью – 2 -3 минуты.
Гликолитический способ образования АТФ имеет ряд преимуществ перед аэробным путем:
- он быстрее выходит на максимальную мощность,
- имеет более высокую величину максимальной мощности,
- не требует участия митохондрий и кислорода.
Однако у этого пути есть и свои недостатки :
- процесс малоэкономичен,
- накопление молочной кислоты в мышцах существенно нарушает их нормальное функционирование и способствует утомлению мышцы.
1. Аэробный путь ресинтеза

Аэробный путь ресинтеза АТФиначе называется тканевым дыханием – это основной способ образования АТФ, протекающий в митохондриях мышечных клеток. В ходе тканевого дыхания от окисляемого вещества отнимаются два атома водорода и по дыхательной цепи передаются на молекулярный кислород, доставляемый в мышцы кровью, в результате чего возникает вода. За счет энергии, выделяющейся при образовании воды, происходит синтез молекул АТФ из АДФ и фосфорной кислоты. Обычно на каждую образовавшуюся молекулу воды приходится синтез трех молекул АТФ.
Кислородная, или аэробная, система является наиболее важной для спортсменов на выносливость, поскольку она может поддерживать физическую работу в течение длительного времени. Кислородная система обеспечивает организм, и в частности мышечную деятельность, энергией посредством химического взаимодействия пищевых веществ (главным образом, углеводов и жиров) с кислородом. Пищевые вещества поступают в организм с пищей и откладываются в его хранилищах для дальнейшего использования по необходимости. Углеводы (сахар и крахмалы) откладываются в печени и мышцах в виде гликогена. Запасы гликогена могут сильно варьироваться, но в большинстве случаев их хватает как минимум на 60-90 мин работы субмаксимальной интенсивности. В то же время запасы жиров в организме практически неисчерпаемы.
Углеводы являются более эффективным "топливом" по сравнению с жирами, так как при одинаковом потреблении энергии на их окисление требуется на 12% меньше кислорода. Поэтому в условиях нехватки кислорода при физических нагрузках энергообразование происходит в первую очередь за счет окисления углеводов.
Поскольку запасы углеводов ограничены, ограничена и возможность их использования в видах спорта на выносливость. После исчерпания запасов углеводов к энергообеспечению работы подключаются жиры, запасы которых позволяют выполнять очень длительную работу. Вклад жиров и углеводов в энергообеспечение нагрузки зависит от интенсивности упражнения и тренированности спортсмена. Чем выше интенсивность нагрузки, тем больше вклад углеводов в энергообразование. Но при одинаковой интенсивности аэробной нагрузки тренированный спортсмен будет использовать больше жиров и меньше углеводов по сравнению с неподготовленным человеком.
Таким образом, тренированный человек будет более экономично расходовать энергию, так как запасы углеводов в организме небезграничны.
Производительность кислородной системы зависит от количества кислорода, которое способен усвоить организм человека. Чем больше потребление кислорода во время выполнения длительной работы, тем выше аэробные способности. Под воздействием тренировок аэробные способности человека могут вырасти на 50%.
Время развертывания составляет 3 – 4 минуты, но у хорошо тренированных спортсменов может составлять 1 мин. Это связано с тем, что на доставку кислорода в митохондрии требуется перестройка практически всех систем организма.
Время работы с максимальной мощностью составляет десятки минут. Это дает возможность использовать данный путь при длительной работе мышц.
По сравнению с другими идущими в мышечных клетках процессами ресинтеза АТФ аэробный путь имеет ряд преимуществ:
- Экономичность: из одной молекулы гликогена образуется 39 молекул АТФ, при анаэробном гликолизе только 3 молекулы.
- Универсальность в качестве начальных субстратов здесь выступают разнообразные вещества: углеводы, жирные кислоты, кетоновые тела, аминокислоты.
- Очень большая продолжительность работы. В покое скорость аэробного ресинтеза АТФ может быть небольшой, но при физических нагрузках она может стать максимальной.
Однако есть и недостатки.
- Обязательное потребление кислорода, что ограничено скоростью доставки кислорода в мышцы и скоростью проникновения кислорода через мембрану митохондрий.
- Большое время развертывания.
- Небольшую по максимальной величине мощность.
Поэтому мышечная деятельность, свойственная большинству видов спорта, не может быть полностью получена этим путем ресинтеза АТФ.
Примечание. Эта глава написана на основе учебника "ОСНОВЫ БИОХИМИИ СПОРТА"
Тема 14. Пути ресинтеза АТФ
| Наименование параметра | Значение |
| Тема статьи: | Тема 14. Пути ресинтеза АТФ |
| Рубрика (тематическая категория) | Все статьи |
1. Анаэробный гликолиз. Ресинтез АТФ в процессе гликолиза. Факторы, влияющие на протекание гликолиза.
2. Аэробный путь ресинтеза АТФ. Особенности регуляции.
3. Ресинтез АТФ в цикле Кребса.
4. Молочная кислота, её роль в организме, пути её устранения.
5. Биологическое окисление. Синтез АТФ при переносе электронов по цепи дыхательных ферментов.
1-й вопрос
Распад глюкозы возможен двумя путями. Один из них состоит в распаде шестиуглероднои̌ молекулы глюкозы на две трехуглеродные. Данный путь называется дихотомическим распадом глюкозы. При реализации второго пути происходит потеря молекулой глюкозы одного атома углерода, что приводит к образованию пентозы; ϶тот путь называется апотомический.
Дихотомический распад глюкозы (гликолиз) может происходить как в анаэробных, так и аэробных условиях. При распаде глюкозы в анаэробных условиях в результате процесса молочнокислого брожения образуется молочная кислота. отдельные реакции гликолиза катализируют 11 ферментов, образующих цепь, в которой продукт реакции, ускоряемой предшествующим ферментом, является субстратом для последующего. Гликолиз условно можно разбить на два этапа. В первом происходит затарта энергии, второй – характеризуется накоплением энергии в виде молекул АТФ.
Химизм процесса представлен в теме ʼʼРаспад углеводовʼʼ и заканчивается переходом ПВК в молочную кислоту.
Бóльшая часть молочнои̌ кислоты, образующейся в мышце, вымывается в кровеносное русло. Изменению рН крови препятствует бикарбонатная буферная система: у спортсменов буферная емкость крови повышена по сравнению с нетренированными людьми, по϶тому они могут переносить более высокое содержание молочнои̌ кислоты. Далее молочная кислота транспортируется к печени и почкам, где почти полностью перерабатывается в глюкозу и гликоген. Незначительная часть молочнои̌ кислоты вновь превращается в пировиноградную кислоту, которая в аэробных условиях окисляется до конечного продукта.
2-й вопрос
Аэробный распад глюкозы иначе называется пентозофосфатным циклом.
Понятие и виды, 2018.
В результате протекания ϶того пути из 6 молекул глюкозо-6-фосфата распадается одна. Апотомический распад глюкозы можно разделить на две фазы: окислительную и анаэробную.
Окислительную фазу где глюкозо-6-фосфат превращается в рибулёзо-5- фосфат представлена в вопросе ʼʼРаспад углеводов. Аэробный распад глюкозыʼʼ
Анаэробная фаза апотомического распада глюкозы.
Дальнейший обмен рибулозо-5-фосфата протекает очень сложно, имеет место превращение фосфопентоз – пентозофосфатный цикл. В результате которого из шести молекул глюкозо-6-фосфата, вступающих в аэробный путь распада углеводов одна молекула глюкозо-6-фосфата полностью расщепляется с образованием СО2, Н2О и 36 молекул АТФ. Именно наибольший энергетический эффект распада глюкозо-6-фосфата, по сравнению с гликолизом (2 молекулы АТФ), имеет важное значение в обеспечении энергией мозга и мышц при физических нагрузках.
3-й вопрос
Цикл ди- и трикарбоновых кислот (цикл Кребса) занимает важное место в процессах обмена веществ: здесь идет обезвреживание ацетил-КоА (и ПВК) до конечных продуктов: углекислого газа и воды; синтезируется 12 молекул АТФ; образуется ряд промежуточных продуктов, которые используются для синтеза важных соединений. К примеру, щавелевоуксусная и кетоглутаровая кислоты могут образовать аспарагиновую и глутаминовую кислоты; ацетил-КоА служит исходным веществом для синтеза жирных кислот, холестерина, холевых кислот, гормонов. Цикл ди- и трикарбоновых кислот является следующим звеном основных видов обмена: обмена углеводов, белков, жиров. Подробно смотри в теме ʼʼРаспад углеводовʼʼ.
4-й вопрос
Увеличение количества молочнои̌ кислоты в саркоплазматическом пространстве мышц сопровождается изменением осмотического давления при ϶том вода из межклеточнои̌ среды поступает внутрь мышечных волокон, вызывая их набухание и регидность. Значительные изменения осмотического давления в мышцах могут быть причинои̌ болевых ощущений.
Молочная кислота легко диффундирует через клеточные мембраны по градиенту концентрации в кровь, где вступает во взаимодействие с бикарбонатнои̌ системой, что приводит к выделению ʼʼнеметаболическогоʼʼ избытка СО2:
NаНСО3 + СН3 – СН – СООН СН3 – СН – СООNа + Н2О + СО2
Исходя из всᴇᴦο выше сказанного, мы приходим к выводу, что увеличение кислотности, повышение СО2, служит сигналом для дыхательного центра, при выходе молочнои̌ кислоты усиливается легочная вентиляция и поставка кислорода работающей мышцы.
5-й вопрос
Биологическое окисление – ϶то совокупность окислительных реакций, происходящих в биологических объектах (в тканях) и обеспечивающих организм энергией и метаболитами для осуществления процессов жизнедеятельности. При биологическом окислении аналогичным образом идет разрушение вредных продуктов обмена веществ, продуктов жизнедеятельности организма.
В развитии теории биологического окисления принимали участие ученые: 1868 г. - Шёнбайн (немецкий ученый), 1897 г. - А.Н. Бах, 1912 г. В.И. Палладин, Г.Виланд. Взгляды этих ученых положены в основу современнои̌ теории биологического окисления. Её суть.
В переносе Н2 на О2 участвуют несколько ферментных систем (дыхательная цепь ферментов), выделяют три основных компонента: дегидрогеназы (НАД, НАДФ); флавиновые (ФАД, ФМН); цитохромы (гем Fe2+). В результате образуется конечный продукт биологического окисления – H2O. В биологическом окислении участвует цепь дыхательных ферментов.
Первый акцептор Н2 – дегидрогеназа, кофермент – либо НАД (в митохондриях), либо НАДФ (в цитоплазме).
| H(H+ē) |
|
|
|
| Субстраты: лактат, цитрат, малат, сукцинат, глицерофосфат и другие метаболиты. В зависимости от природы организма и окисляемого субстрата окисление в клетках может осуществляться главным образом по одному из 3-х путей. 1.При полном наборе дыхательных ферментов, когда идет предварительное активирование О в О2-. Н (Н+е-) Н+е- 2е- 2е- 2е- 2е- 2е- S НАД ФАД b c a1 a3 1/2O2 H2O Н (Н+е-) Н+е- 2.Без цитохромов: S НАД ФАД О2 Н2О2. 3.Без НАД и без цитохромов: S ФАД О2 Н2О2. Учёные установили, что при переносе водорода на кислород при участии всех переносчиков образуется три молекулы АТФ. Восстановление формы НАД·H2 и НАДФ·H2 при переносе H2 на O2 дают 3 АТФ, а ФАД·H2 даёт 2 АТФ. При биологическом окислении образуется Н2О или Н2О2, она, в свою очередь, под действием каталазы распадается на Н2О иО2. Вода, образующаяся при биологическом окислении, расходуется на нужды клетки (реакции гидролиза) или выводится как конечный продукт из организма. При биологическом окислении выделяется энергия, которая либо переходит в тепловую и рассеивается, либо накапливается в ~ АТФ и потом используется на все жизненные процессы. Процесс, при котором идет накопление энергии, освободившейся при биологическом окислении, в ~ связях АТФ – окислительное фосфорилирование, то есть синтез АТФ из АДФ и Ф(н) за счёт энергии окисления органических веществ: Н+ внешняя сторона ОН- матрикс Мембрана оказывается поляризованнои̌. С наружнои̌ стороны мембраны накапливаются ионы Н+, а с внутренней – ионы ОН-. Вследствие того, что по обе стороны мембраны находятся разнозаряженные частицы возникает электрохимический мембранный потенциал, который является движущей силой для синтеза АТФ. Синтез АТФ катализируется АТФ-синтетазой, расположеннои̌ в мембране. АДФ + Ф(н) АТФ + Н+ + ОН- АТФ будет синтезироваться, в случае если образующаяся вода будет удаляться. Это достигается благодаря тому, что в силу градиента рН ионы ОН- воды вытягиваются в наружнее пространство, а ионы Н+ - во внутреннее пространство митохондрий. При переносе пары е- во внешнее пространство выбрасывается 6 протонов (Н+), что приводит к образованию 3-х молекул АТФ. Тема 14. Пути ресинтеза АТФ - понятие и виды. Классификация и особенности категории "Тема 14. Пути ресинтеза АТФ"2017-2018. |
Человека, для того чтобы постоянно поддерживать работоспособность и жизнедеятельность мышечных тканей.
Выделение необходимых элементов и кислот при течении ресинтеза обеспечивает возможность, к примеру спортсменам, на протяжении долгого периода держать мышечную ткань в напряжении.
Находясь в покое, для поддержания своего состояния и текущих процессов метаболизма, мышцам необходим постоянный ресинтез АТФ и выработка соответствующих .
Механизм возникновения аденозинтрифосфата представляет собой процесс, который должен постоянно происходить в организме человека, для обеспечения работоспособности мышц в состоянии покоя. При этом, потребление ими аденофосфатов возрастает, в тот момент, когда происходит сокращение мускулатуры.
Ресинтез АТФ поставляет тканям необходимую энергию для работоспособности и актомиозиновый комплекс элементов, а в активном состоянии обеспечивает их необходимым количеством ионами кальция.
Для этого количество аденозитрофосфорной в мышечных тканях постоянно восстанавливается. При этом оперативность восстановления равняется времени потребления, этот процесс происходит за счет определенных биохимических механизмов ресинтеза.
Элементами, выступающими в роли источников протекаемого ресинтеза АФТ в организме, могут быть мышцы «костяка» и некоторые другие ткани. Именно эти энергетические источники богаты фосфатосодержащими элементами:
- Креатинофосфатом
- Аденозинфосфатом
Помимо этого, в процессе катаболизма, образуются:
- Гликоген
- Энергетические компоненты
По итогам протекания процесса окисления в аэробной среде, в организме возникают элементы градиента. В мышцах располагается примерно 0,20% АТФ, при этом возрастает значение концентрации «%», и угнетение миозиновой массы, вследствие чего, обеспечивается исключение возникновения мышечных спаек.
Но концентрация содержания в мышцах АТФ не должна снижаться, менее 0,1%, в противном случае мышцы будут сокращаться до своего полного истощения. Это обеспечивается за счет того, что в этот момент перестает работать кальциевая в саркоплазматической ретикулума.
В случае истощения мышцы, начинает развиваться ригора, т. е. системное не проходящее сокращение.
Анаэробные и аэробные процессы ресинтеза в мышцах

Ресинтез АТФ – это реакция с условиями аэробных и анаэробных механизмов.
Протекание реакции, в активный период, может проходить, как в результате реакции, при наличии анаэробных условий.
Анаэробные процесс ресинтеза протекают без участия кислорода, при условии наличия кислорода – реакция называется аэробная.
При постоянных показателях, ресинтез АТФ протекает, с участием кислорода, следовательно, наблюдается аэробный процесс.
Вследствие напряженного физического труда процесс ресинтеза АТФ не происходит, так как доступ кислорода к мышцам исключен. В мышцах «костяка» наблюдаются всего три анаэробных и один аэробный – восстановление аденозинтрифосфата.
Подобный процесс включает в себя такие механизмы, как:
- Креатинфосокиназный
- Алактатный
- Лактатный
- Миокиназный
Непосредственно протекание аэробного включает себя течение окислительного фосфалирования, количество митохондрий при этом значительно повышается. При аэробном окислении, наблюдается выработка энергетического субстрата:
- Глюкоза
- Жирные кислоты
- Некоторые аминокислоты
- Молочная кислота
- Кетоновые тела
Аэробный механизм или, как его еще называют кислотный, представляет собой важный процесс для спортсменов, так как обеспечивает скорость и выносливость. Именно аэробная реакция может поддерживать в постоянном напряжении на протяжении длительного периода времени.
Кислородные реакции в мышцах обеспечивают их работоспособность энергией, в основном, за счет химического взаимодействия таких пищевых веществ, как жиры и углеводы непосредственно с кислородом. Все нужные компоненты поступают в организм спортсмена совместно с пищей и накапливаются в запасниках до момента пока будут необходимы.
К примеру, сахар и крахмал, которые выступают в роли углеводов, образуют элемент – гликоген. В среднем, в организме человека гликоген может до 70-80 минут обеспечивать работу субмаксимальной работоспособности. Но при этом уровень жиров в организме никогда не исчерпывается.
Именно, углеводы являются самым из энергопоставщиков для организма, если сравнивать с жирами.
Это обусловлено тем, что при одинаковом потреблении, для их окисления требуется на 10% меньше кислорода. Этот факт является очень актуальным для ситуаций с нехваткой кислорода при сильных физических нагрузках.
В связи с тем, что запасы углеводов в организме с течением времени имеют свойство исчерпываться, выносливость и достижения (возможности) спортсменов снижаются. После того, как будут исчерпаны все запасы – к процессу поддержания, подключаются жиры и подпитывают бесперебойную работоспособность.
Собственно, вклад таких компонентов, как жиры и углеводы в обеспечение мышц энергией, напрямую зависит от работоспособности и уровня затрачиваемой энергии.
Но, при одной и той же интенсивности нагрузки, в условиях аэробной реакции, организм будет потреблять меньшее количество углеводов и больший уровень жиров. Это правило в основном действует для спортсменов, так как их мышцы систематически подвергаются нагрузкам, если сравнивать с неподготовленными людьми.
Таким образом, можно сделать вывод, что человек с тренированными мышцами расходует намного меньшее количество энергии, так как имеет в организме большие углеводов.
Кислородная система может производить столько кислорода, сколько, может потреблять организм, и чем более высок уровень потребления, в момент выполнения напряженной работы, тем больше растет эффективность. В сравнении с происходящими аналоговыми реакциями, процессами ресинтеза АТФ, именно аэробный механизм характеризуется большими преимуществами:
- Высокий уровень экономичности, так как из одной молекулы возникает 30 молекул АТФ, в сравнении с анаэробным процессом, в котором образуется только 3 молекулы.
- Многофункциональность, так как в качестве энергетических компонентов выступают аминокислоты, углеводы, кетоновые тела и .
- Значительно большая продолжительность работы процесса, так как в момент покоя, ресинтез АТ сравнительно небольшой, но при увеличении нагрузок – он моментально растет до максимального показателя.
Но, при явных достоинствах, аэробный процесс характеризуется и некоторыми недостатками:
- Постоянное потребление молекул кислорода, значительно лимитирует скорость его прохождения к мышцам и процесс его всасывания по средствам мембраны метохондрий.
- Большой показатель развертывания по времени.
- Минимальный показатель максимальной мощности.
В мышцах в ходе ресинтеза АФТ протекают определенные процессы. Самый важный и быстрый – креатинкиназная реакция, которая вырабатывает фофорильные элементы, при исчерпании АТФ.
В среде с небольшим показателем кислотности в основном происходит активация элементов дыхания и в то же время возникает угнетение ферментов, отвечающих за работы мышечных тканей и реакции ресинтеза АТФ. В самом начале процесса происходит перенос АТФ в межмембранное пространство, используя внутреннюю мембрану.
В этот момент ресинтез АТФ является связующим между креатином, проникающим из краетинкиназы. Именно такое взаимодействие способствует метахондриальной креатинкиназы, которая располагается во мембране митохондрий и тем самым образуется креатиносфат.
Таким образом, возникающий элемент снова попадает в саркоплазму, в которой отторгает остаток элементов фофора с АТФ на саркоплазматическую АДФ.
Максимальный период протекания процесса не превышает 30 секунд, а максимальная мощность достигается за 2 минуты.
Данный метод характеризуется преимуществами, в сравнении с аналогами:
- Намного быстрее достигается максимальная мощность
- Показатель максимальной мощности намного больше, чем у аэробного способа
- Происходит без необходимости использовать кислород и митохондрии
Хотя, даже гликолитический способ имеет и ряд недостатков:
- Механизм имеет небольшой показатель экономичности
- Большое скопление кислоты в мышцах может навредить их стандартному функционированию и даже стимулировать их утомление
Миокиназный механизм протекает при большом количестве АДФ в саркоплазме и возникает, как вспомогательный метод, при условиях, что остальные возможности уже исчерпали себя и в данный момент уже близки к этому показателю.

Миокиназная в тканях чаще всего возникает при значительном повышении уровня АДФ.
В основном такая ситуация может возникать при сильной мышечной усталости.
Таким словом, можно сказать, происходящие аэробные и анаэробные реакции, обеспечивают высокий требуемый уровень энергии.
Общие показатели и энергетические возможности протекающих реакций
Ресинтез АТФ протекает и собственно сам входящий механизм характеризуется отличными друг от друга показателями энергообеспечения, которые протекают исходя из таких критериев:
- «Мах» мощность
- Быстрота протекания
- Емкость по показателю матеболизма
- «Мах» эффективность
«Мах» является наибольшим значением скорости возникновения элементов АТФ, в одном из метаболических реакций, которая ограничивает лимит интенсивности выполняемых действий, благодаря применяемым особенностям механизма реакции. протекания обуславливает максимальное время, за которое достигается наивысший уровень мощности ресинтеза аденозинтрифосфата.
Метаболическая емкость является показателем целостного значения АТФ, которое может возникать в процессе использования цепочки происходящих процессов ресинтеза АТФ, учитывая значение постоянного количества элементов обеспечивающих поставки энергии в мышцы.
Полномерное количество емкости своим количеством ограничивает объем выполняемого действия. Таким образом, подобная эффективность протекает ограниченной количеством энергии, которая скапливается в макроэргитических связях аденозитрифосфата.
Именно, эта характеризует экономичность проделываемой в этот момент работы и в данном случае критерием служит общий показатель полезного действия.
Значение коэффициента полезного действия, в таком случае будет представлять собой отношение общего показателя полезной затрачиваемой энергии, к ее общему количеству, которое возникает в ходе вышеуказанного процесса. Общий коэффициент ПД при метаморфозах энергии, при метаболических процессах, в основном зависит, от:
- Уровня фосфолирования
- Показателя хемомеханических процессов
«Мах» эффективность таких хемомеханических сопряжений протекает практически одинаково и составляет 1\2 общей реакции.
«Мах» эффективность уровня фосфолирования является наивысшим значением в алактатном анаэробном процессе, и составляет 80%, и минимальный показатель – 40%, при возникновении реакции гликолиза – увеличивается до 42%. В стационарном аэробном процессе показатель равняется 58%.
Таким образом, можно сделать вывод, что процессы при анаэробных условиях характеризуются значительно увеличенной максимальной мощностью возникновения АТФ, но при этом имеют практически минимальный период удержания накопленных компонентов.
О том, что такое синтез АТФ, можно посмотреть на видео::
Мышцы – главный биохимический преобразователь химической энергии АТФ непосредственно в механическую энергию сокращения и движения. Мышечная ткань занимает первое место по объёму среди других тканей человека; на её долю при рождении приходится чуть меньше 25%, у людей среднего возраста – более 40%, у пожилых – чуть меньше 30%, а у спортсменов, наращивающих мускулатуру – 60% и более от общей массы тела.
Эффективное преобразование химической энергии в механическую возможно при соблюдении ряда условий:
1) должно быть обеспечено постоянное снабжение химической энергией. В мышцах человека химическая энергия заключена в молекулах АТФ и КрФ;
2) должны существовать средства регуляции механической активности – скорости, длительности и силы сокращения;
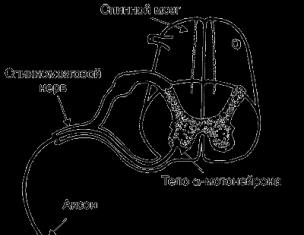
3) процесс преобразования должен находиться под контролем оператора – нервной системы;
4) для того, чтобы система преобразования энергии могла использоваться многократно, необходим механизм возврата системы в исходное состояние.
В настоящее время мышца рассматривается как высокоэффективная, универсальная машина, которая «тянет», но не «толкает», следовательно, каждая мышца должна находиться под антагонистическим воздействием другой группы мышц или какой-либо иной силы, такой, как сила тяжести или эластичная отдача.
Обе фазы мышечной деятельности – сокращение и расслабление – протекают при обязательном использовании энергии, которая выделяется при гидролизе АТФ. Однако запасы АТФ в мышечных клетках незначительны и их достаточно для мышечной работы в течение 1 – 2 секунд. Поэтому для обеспечения более продолжительной мышечной деятельности в мышцах должно происходить пополнение запасов АТФ. Образование АТФ в мышечных клетках непосредственно во время физической работы называется ресинтезом АТФ и идёт с потреблением энергии. В зависимости от источника энергии выделяют несколько путей ресинтеза АТФ.
Для количественной характеристики различных путей ресинтеза АТФ обычно используются следующие критерии:
1) максимальная мощность, или максимальная скорость, – это наибольшее количество АТФ, которое может образоваться в единицу времени за счёт данного пути ресинтеза. Измеряется максимальная мощность в калориях или джоулях, исходя из того, что 1 ммоль АТФ соответствует в физиологических условиях примерно 12 кал или 50 Дж. Поэтому данный критерий имеет размерность кал/мин×кг мышечной ткани или соответственно Дж/мин×кг мышечной ткани.
2) время развертывания – это минимальное время, необходимое для выхода ресинтеза АТФ на свою наибольшую скорость, т.е. для достижения максимальной мощности. Этот критерий измеряется в единицах времени (с, мин).
3) время сохранения или поддержания максимальной мощности – это наибольшее время функционирования данного пути ресинтеза АТФ с максимальной мощностью. Единицы измерения – с, мин, ч.
4) метаболическая емкость – общее количество АТФ, которое может образоваться во время мышечной работы за счёт данного пути ресинтеза АТФ.
В зависимости от потребления кислорода пути ресинтеза АТФ делятся на аэробные и анаэробные.
АЭРОБНЫЙ ПУТЬ РЕСИНТЕЗА АТФ
Аэробный путь ресинтеза АТФ (тканевое дыхание) – основной, базовый способ образования АТФ, протекающий в митохондриях мышечных клеток. В ходе тканевого дыхания от окисляемого вещества отнимаются два атома водорода и по дыхательной цепи передаются на молекулярный кислород, доставляемый кровью в мышцы из воздуха, в результате чего возникает вода. За счёт энергии, выделяющейся при образовании воды, происходит синтез АТФ из АДФ и фосфорной кислоты. Обычно на каждую образовавшуюся молекулу воды приходится синтез трёх молекул АТФ.
Скорость аэробного пути ресинтеза АТФ контролируется содержанием в мышечных клетках АДФ, который является активатором ферментов тканевого дыхания. В состоянии покоя, когда в клетках почти нет АДФ, тканевое дыхание протекает с очень низкой скоростью. При мышечной работе за счёт интенсивного использования АТФ происходит образование и накопление АДФ. Появившийся избыток АДФ ускоряет тканевое дыхание, и оно может достигнуть максимальной интенсивности.
Другим активатором аэробного пути ресинтеза АТФ является углекислый газ. Возникая при физической работе в избытке, он активирует дыхательный центр мозга, что в итоге приводит к повышению скорости кровообращения и улучшению снабжения мышц кислородом.
Аэробный путь образования АТФ характеризуется следующими критериями. Максимальная мощность составляет 350 – 450 кал/мин×кг. По сравнению с анаэробными путями ресинтеза АТФ тканевое дыхание обладает самой низкой величиной максимальной мощности. Это обусловлено тем, что возможности аэробного процесса ограничены доставкой кислорода в митохондрии и их количеством в мышечных клетках. Поэтому за счёт аэробного пути ресинтеза АТФ возможно выполнение физических нагрузок только умеренной мощности.
Время развёртывания – 3 – 4 мин (у хорошо тренированных спортсменов может быть около 1 мин). Такое большое время развёртывания объясняется тем, что для обеспечения максимальной скорости тканевого дыхания необходима перестройка всех систем организма, участвующих в доставке кислорода в митохондрии мышц.
Время работы с максимальной мощностью составляет десятки минут. Источниками энергии для аэробного ресинтеза АТФ являются углеводы, жиры и аминокислоты, распад которых завершается циклом Кребса. Причём для этой цели используются не только внутримышечные запасы данных веществ, но и углеводы, жиры, кетоновые тела и аминокислоты, доставляемые кровью в мышцы во время физической работы. В связи с этим данный путь ресинтеза АТФ функционирует с максимальной мощностью в течение такого продолжительного времени.
По сравнению с другими идущими в мышечных клетках процессами ресинтеза АТФ аэробный ресинтез имеет ряд преимуществ. Он отличается высокой экономичностью: в ходе этого процесса идёт глубокий распад окисляемых веществ до конечных продуктов – углекислого газа и воды, поэтому выделяется большое количество энергии. Другим достоинством этого пути ресинтеза является универсальность в использовании субстратов. В ходе аэробного ресинтеза окисляются все основные органические вещества организма: белки, углеводы, жирные кислоты и др. Ещё одним преимуществом этого способа образования АТФ является очень большая продолжительность его работы: практически он функционирует постоянно в течение всей жизни.
Однако аэробный способ образования АТФ имеет и ряд недостатков. Так, действие этого способа связано с обязательным потреблением кислорода, доставка которого в мышцы обеспечивается дыхательной и сердечно-сосудистой системами (вместе они обозначаются термином «кардиореспираторная система»). Функциональное состояние кардиореспираторной системы является лимитирующим фактором, ограничивающим продолжительность работы аэробного пути ресинтеза АТФ с максимальной мощностью и величину самой максимальной мощности. Возможности аэробного пути ограничены ещё и тем, что все ферменты тканевого дыхания встроены во внутреннюю мембрану митохондрий в форме дыхательных ансамблей и функционируют только при наличии неповреждённой мембраны. Любые факторы, влияющие на состояние и свойства мембран, нарушают образование АТФ аэробным способом. Ещё одним недостатком аэробного образования АТФ можно считать большое время развёртывания (3 – 4 мин) и небольшую по абсолютной величине максимальную мощность. В спортивной практике для оценки аэробного фосфорилирования часто используют три показателя: максимальное потребление кислорода (МПК), порог анаэробного обмена (ПАНО), кислородный приход.
МПК – максимально возможная скорость потребления кислорода организмом при выполнении физической работы. Этот показатель характеризует максимальную мощность аэробного пути ресинтеза АТФ: чем выше величина МПК, тем больше значение максимальной скорости тканевого дыхания, это обусловлено тем, что практически весь поступающий в организм кислород используется в этом процессе. МПК представляет собой интегральный показатель, зависящий от многих факторов: от функционального состояния кардиореспираторной системы, от содержания в крови гемоглобина, от количества и размера митохондрий. У нетренированных молодых людей МПК обычно равно 3 – 4 л/мин, у спортсменов высокого класса, выполняющие аэробные нагрузки, МПК – 6 – 7 л/мин. На практике, для исключения влияния на эту величину массы тела МПК рассчитывают на кг массы тела. В этом случае у молодых людей, не занимающихся спортом, МПК равно 40 – 50 мл/мин×кг, а у хорошо тренированных спортсменов – 80 – 90 мл/мин×кг.
ПАНО – минимальная относительная мощность работы, измеренная по потреблению кислорода в процентах по отношению к МПК, при которой начинает включаться гликолитический путь ресинтеза АТФ. У нетренированных ПАНО составляет 40 – 50% от МПК, а у спортсменов ПАНО может достигать 70% от МПК.
Кислородный приход – это количество кислорода, использованное во время выполнения данной нагрузки для обеспечения аэробного ресинтеза АТФ. Кислородный приход характеризует вклад тканевого дыхания в энергообеспечение проделанной работы.
КРЕАТИНФОСФАТНЫЙ ПУТЬ ОБРАЗОВАНИЯ АТФ
Анаэробные пути ресинтеза АТФ являются дополнительными способами образования АТФ в тех случаях, когда основной путь получения АТФ – аэробный – не может обеспечить мышечную деятельность необходимым количеством энергии. Это бывает на первых минутах любой работы, когда тканевое дыхание ещё полностью не развернулось, а также при выполнении физических нагрузок высокой мощности.
В мышечных клетках всегда имеется креатинфосфат – соединение, содержащее фосфатную группу, связанную с остатком креатина макроэргической связью. Содержание КрФ в мышцах в покое – 15 – 20 ммоль/кг.
КрФ обладает большим запасом энергии и высоким сродством к АДФ. Поэтому он легко вступает во взаимодействие с молекулами АДФ, появляющимися в мышечных клетках при физической работе в результате гидролиза АТФ. В ходе этой реакции остаток фосфорной кислоты с запасом энергии переносится с КрФ на молекулу АДФ с образованием креатина и АТФ. Эта реакция катализируется ферментом креатинкиназой. В связи с этим данный путь ресинтеза АТФ ещё называют креатинкиназным. Креатинфосфатная реакция обратима, но её равновесие смещено в сторону образования АТФ, и поэтому она начинает осуществляться сразу же, как только в миоцитах появляются первые порции АДФ.
При мышечной работе активность креатинкиназы значительно возрастает за счёт активирующего воздействия на неё ионов кальция, концентрация которых в саркоплазме под действием нервного импульса увеличивается почти в 1000 раз. Другой механизм регуляции креатинфосфатной реакции связан с активирующим воздействием на креатинкиназу креатина, образующегося в ходе данной реакции. За счёт этих механизмов активность креатинкиназы в начале мышечной работы резко увеличивается и креатинфосфатная реакция очень быстро достигает максимальной скорости.
Креатинфосфат, обладая большим запасом химической энергии, является веществом непрочным. От него легко может отщепляться фосфорная кислота, в результате чего происходит циклизация остатка креатина, приводящая к образованию креатинина, которое происходит без участия ферментов, спонтанно. Образовавшийся креатинин в организме не используется и выводится с мочой. Поэтому по выделению креатинина с мочой можно судить о содержании креатинфосфата в мышцах, так как в них находятся основные запасы этого соединения.
Синтез креатинфосфата в мышечных клетках происходит во время отдыха путём взаимодействия креатина с избытком АТФ. Частично запасы КрФ могут восстанавливаться и при мышечной работе умеренной мощности, при которой АТФ синтезируется за счёт тканевого дыхания в таком количестве, которого хватает и на обеспечение сократительной функции миоцитов, и на восполнение запасов креатинфосфата. Поэтому во время выполнения физической работы креатинфосфатная реакция может включаться многократно.
Образование креатина в печени происходит с использованием трёх аминокислот: глицина, метионина и аргинина. В спортивной практике для повышения в мышцах концентрации КрФ используют в качестве пищевых добавок препараты глицина и метионина. Креатинфосфатный путь ресинтеза АТФ характеризуется следующими величинами принятых количественных критериев:
Максимальная мощность составляет 900 – 1100 кал/мин×кг, что в три раза выше соответствующего показателя для аэробного ресинтеза. Такая большая величина обусловлена высокой активностью фермента креатинкиназы и, следовательно, очень высокой скоростью креатинфосфатной реакции.
Время развёртывания всего 1 – 2 секунды. Исходных запасов АТФ в мышечных клетках хватает на обеспечение мышечной деятельности как раз в течение 1 – 2 с, и к моменту их исчерпания креатинфосфатный путь образования АТФ уже функционирует со своей максимальной скоростью. Такое малое время развёртывания объясняется действием механизмов регуляции активности креатинкиназы, позволяющих резко повысить скорость этой реакции.
Время работы с максимальной скоростью всего лишь 8 – 10 с, что связано с небольшими исходными запасами креатинфосфата в мышцах.
Главными преимуществами креатинфосфатного пути образования АТФ являются очень малое время развёртывания и высокая мощность, что имеет крайне важное значение для скоростно-силовых видов спорта. Главным недостатком этого способа синтеза АТФ, существенно ограничивающим его возможности, является короткое время его функционирования. Время поддержания максимальной скорости всего 8 – 10 с, к концу 30-й его скорость снижается вдвое. А к концу 3-й минуты интенсивной работы креатинфосфатная реакция в мышцах практически прекращается.
Исходя из такой характеристики креатинфосфатного пути ресинтеза АТФ, следует ожидать, что эта реакция окажется главным источником энергии для обеспечения кратковременных упражнений максимальной мощности. Креатинфосфатная реакция может неоднократно включаться во время выполнения физических нагрузок, что делает возможным быстрое повышение мощности выполняемой работы, развития ускорения на дистанции и финишный рывок.
ИНСУЛИН И ОБМЕН ГЛЮКОЗЫ
Поджелудочная железа, по сути дела, представляет собой два разных органа, объединённых в единую морфологическую структуру. Её ацинарная часть выполняет экзокринную функцию, секретируя в просвет двенадцатиперстной кишки ферменты и ионы, необходимые для процессов пищеварения. Эндокринная часть железы состоит из 1 – 2 млн. островков Лангерганса, на долю которых приходится 1 – 2% всей массы поджелудочной железы. Островки в поджелудочной железе были обнаружены в 1860 году. Лангерганс, которому принадлежит это открытие, не представлял себе, что удаление поджелудочной железы ведёт к сахарному диабету. Это было доказано в 1921 году Бантингом и Бестом. Экстрагировав подкисленным этанолом ткань поджелудочной железы, они выделили некий фактор, обладающий мощным гипогликемизирующим действием. Этот фактор был назван инсулином. Вскоре было установлено, что инсулин, содержащийся в островках поджелудочной железы крупного рогатого скота и свиней, активен и у человека. Инсулин во многих отношениях может служить моделью пептидных гормонов. Он первым из гормонов этой группы был получен в очищенном виде, кристаллизован и синтезирован химическим путём и методами генной инженерии. Исследование путей биосинтеза привело к созданию концепции пропептидов.
Молекула инсулина – полипептид, состоящий из двух цепей, А и В, связанных между собой двумя дисульфидными мостиками, соединяющими остаток А7 с остатком В7 и остаток А20 с остатком В19. Третий дисульфидный мостик связывает между собой остатки 6 и 11 А-цепи. Локализация всех трёх дисульфидных мостиков постоянна, а А- и В-цепи у представителей большинства видов имеют по 21 и 30 аминокислот соответственно. Молекулярная масса человеческого инсулина 5734. В обеих цепях во многих положениях встречаются замены, не оказывающие влияние на биологическую активность гормона, однако наиболее часты замены по положениям 8,9 и 10 А-цепи. Из этого следует, что данный участок не имеет критического значения для биологической активности инсулина. Однако некоторые участки и области молекулы инсулина обладают высокой консервативностью. К ним относятся 1) положения трёх дисульфидных мостиков 2) гидрофобные остатки в С-концевом участке В-цепи 3) С- и N-концевые участки А-цепи. Использование химических модификаций и замен отдельных аминокислот шести этих участков помогает идентифицировать сложный активный центр.
Синтез инсулина и его упаковка в гранулы происходит в определённом порядке. Проинсулин синтезируется на рибосомах шероховатого эндоплазматического ретикулума. Затем в цистернах этой органеллы происходит ферментативное отщепление лидерной последовательности, образование дисульфидных мостиков и складывание молекулы. После этого молекула инсулина переносится в аппарат Гольджи, где начинается протеолиз и упаковка в секреторные гранулы. Созревание гранул продолжается по мере продвижения по цитоплазме в направлении плазматической мембраны.
Поджелудочная железа человека секретирует 40 – 50 ед. инсулина в сутки, что соответствует 15 – 20% общего количества гормона в железе. Секреция инсулина – энергозависимый процесс, происходящий с участием системы микротрубочек и микрофиламентов островковых В-клеток и ряда медиаторов.
Повышение концентрации глюкозы в крови – главный физиологический стимул секреции инсулина. Пороговой для секреции инсулина является концентрация глюкозы натощак 80 – 100 мг%, а максимальная реакция достигается при концентрации глюкозы 300 – 500 мг%. Секреция инсулина в ответ на повышение концентрации глюкозы носит двухфазный характер. Немедленный ответ, или первая фаза реакции, начинается в пределах 1 минуты после повышения концентрации глюкозы и продолжается в течение 5 – 10 мин. Затем наступает более медленная и продолжительная вторая фаза, обрывающаяся сразу после удаления глюкозного стимула. Согласно существующим представлениям, наличие двух фаз ответной реакции инсулина отражает существование двух различных внутриклеточных пулов инсулина. Абсолютная концентрация глюкозы в плазме – не единственная детерминанта секреции инсулина. В-клетки реагируют и на скорость изменения концентрации глюкозы в плазме.
Внутриклеточная концентрация свободной глюкозы значительно ниже её внеклеточной концентрации. Большинство имеющихся данных свидетельствуют о том, что скорость транспорта глюкозы через плазматическую мембрану мышечных и жировых клеток определяет интенсивность фосфорилирования глюкозы и её дальнейший метаболизм. D-глюкоза и другие сахара с аналогичной конфигурацией проникают в клетки путём облегчённой диффузии, опосредованной переносчиком. Во многих клетках инсулин усиливает этот процесс, что обусловливается увеличением числа переносчиков, а не повышением сродства связывания. В жировых клетках это происходит путём мобилизации переносчиков глюкозы из неактивного их пула в АГ с дальнейшим направлением их к активному участку плазматической мембраны.
Инсулин оказывает влияние на внутриклеточную утилизацию глюкозы различными путями. В норме примерно половина поглощённой глюкозы вступает на путь гликолиза и превращается в энергию, другая половина запасается в виде жиров или гликогена. В отсутствие инсулина ослабевает интенсивность гликолиза и замедляются анаболические процессы гликогенеза и липогенеза. Действительно, при дефиците инсулина всего лишь 5% поглощённой глюкозы превращается жир.
Инсулин усиливает интенсивность гликолиза в печени, повышая активность и концентрацию ряда ключевых ферментов, таких как, глюкокиназа, фосфофруктокиназа и пируваткиназа. Более интенсивный гликолиз сопровождается более активной утилизацией глюкозы и, следовательно, косвенно способствует снижению выхода глюкозы в плазму. Инсулин, кроме того, подавляет активность глюкозо-6-фосфатазы – фермента, обнаруживаемого в печени, но не в мышцах. В результате глюкоза удерживается в печени, так как для глюкозо-6-фосфата плазматическая мембрана непроницаема.
В жировой ткани инсулин стимулирует липогенез путём 1) притока ацетил-СоА и NADFH, необходимых для синтеза жирных кислот, 2) поддержания нормального уровня фермента ацетил-СоА-карбоксилазы, катализирующего превращение ацетил-СоА в малонил-Соа, и 3) притока глицерола, участвующего в синтезе триацилглицеролов. При инсулиновой недостаточности все эти процессы ослабляются и в результате интенсивность липогенеза снижается.
Механизм влияния инсулина на утилизацию глюкозы включает в себя и другой анаболический процесс. В печени и в мышцах инсулин стимулирует превращение глюкозы в гл-6-ф, который затем подвергается изомеризации в гл-1-ф и в таком виде включается в гликоген под действием фермента гликогенсинтазы. Это действие имеет двойственный и непрямой характер. В результате высвобождение глюкозы из гликогена снижается.
Влияние инсулина на транспорт глюкозы, гликолиз и гликогенез проявляется за считанные секунды или минуты, поскольку первичные реакции этого влияния сводятся к активации или инактивации ферментов путём их фосфорилирования или дефосфорилирования. Более продолжительное влияние инсулина на содержание глюкозы в плазме крови связано с ингибированием глюконеогенеза. Образование глюкозы из предшественников неуглеводной природы осуществляется в результате ряда ферментативных реакций, многие из которых стимулируются глюкагоном, глюкокортикоидными гормонами и в меньшей степени ангиотензином и вазопрессином. Инсулин же подавляет данные ферментативные реакции.
Результирующее действие всех перечисленных выше эффектов инсулина сводится к снижению содержания глюкозы в крови. Этому действию инсулина противостоят эффекты целого ряда гормонов, что, несомненно, отражает один из важнейших защитных механизмов организма, поскольку длительная гипогликемия способна вызвать несовместимые с жизнью изменения в мозге и, следовательно, её нельзя допускать.
ГЛИКОЛИТИЧЕСКИЙ ПУТЬ РЕСИНТЕЗА АТФ
Этот путь ресинтеза, так же как и креатинфосфатный, относится к анаэробным способам образования АТФ. Источником энергии, необходимой для ресинтеза АТФ, является мышечный гликоген, концентрация которого в саркоплазме колеблется в пределах 0,2 – 3%. При анаэробном распаде гликогена от его молекулы под воздействием фермента фосфорилазы поочерёдно отщепляются концевые остатки глюкозы в форме гл-1-ф. Далее молекулы гл-1-ф через ряд последовательных стадий превращаются в молочную кислоту. В процессе гликолиза образуются промежуточные продукты, содержащие фосфатную группу с макроэргической связью, которая легко переносится на АДФ с образованием АТФ. Все ферменты гликолиза находятся в саркоплазме мышечных клеток.
Регуляция скорости гликолиза осуществляется путём изменения активности двух ферментов: фосфорилазы и фосфофруктокиназы. Фосфорилаза катализирует первую реакцию распада гликогена – отщепление от него гл-1-ф. Этот фермент активируется адреналином, АМФ и ионами кальция, а ингибируется гл-6-ф и избытком АТФ. Второй регуляторный фермент гликолиза – фосфофруктокиназа – активируется АДФ и особенно АМФ, а тормозится избытком АТФ и лимонной кислотой. Наличие таких регуляторных механизмов приводит к тому, что в покое гликолиз протекает очень медленно, при интенсивной мышечной работе его скорость резко возрастает и может увеличиваться по сравнению с уровнем покоя почти в 2000 раз.
Количественные критерии гликолитического пути ресинтеза АТФ:
Максимальная мощность – 750 – 850 кал/мин×кг, что примерно вдвое выше соответствующего показателя тканевого дыхания. Высокое значение максимальной мощности гликолиза объясняется содержанием в мышечных клетках большого запаса гликогена, наличием механизмов активации ключевых ферментов, приводящих к значительному росту скорости гликолиза, отсутствием потребности в кислороде.
Время развёртывания – 20 – 30 с. Это обусловлено тем, гликоген и ферменты находятся в саркоплазме миоцитов, а также возможностью активации ферментов гликолиза. Фосфорилаза – фермент, запускающий гликолиз, - активируется адреналином, который выделяется в кровь непосредственно перед началом работы. Ионы кальция, концентрация которых в саркоплазме повышается примерно в 1000 раз под воздействием двигательного нервного импульса, также являются мощными активаторами фосфорилазы.
Время работы с максимальной мощностью – 2 – 3 минуты. Существуют две основные причины такой небольшой величины этого критерия. Во-первых, гликолиз протекает с высокой скоростью, что быстро приводит к уменьшению в мышцах концентрация гликогена и, следовательно, к последующему снижению скорости его распада. Во-вторых, в процессе гликолиза образуется молочная кислота, накопление которой приводит к повышению кислотности внутри мышечных клеток. В условиях повышенной кислотности снижается каталитическая активность ферментов, в том числе ферментов гликолиза, что также ведёт к уменьшению скорости данного пути ресинтеза АТФ.
Гликолитический способ образования АТФ имеет ряд преимуществ перед аэробным путём. Он быстрее выходит на максимальную мощность (20-30 с), имеет более высокую величину максимальной мощности (в 2 раза больше) и не требует участия митохондрий и кислорода.
Однако у этого пути есть существенные недостатки. Этот процесс малоэкономичен. Распад до лактата одного остатка глюкозы, отщеплённого от гликогена, даёт только 3 молекулы АТФ, тогда как при аэробном окислении гликогена до воды и углекислого газа образуется 39 молекул АТФ в расчёте на один остаток глюкозы. Такая неэкономичность в сочетании с большой скоростью быстро приводит к исчерпанию запасов гликогена. Другой серьёзный недостаток гликолитического пути – образование и накопление лактата, являющегося конечным продуктом этого процесса. Накопление лактата в мышечных клетках существенно влияет на их функционирование. В условиях повышенной кислотности, вызванной нарастанием концентрации лактата, снижается сократительная способность белков, участвующих в мышечной деятельности, уменьшается каталитическая активность белков-ферментов, в том числе АТФазная активность миозина и активность кальциевой АТФазы, изменяются свойства мембранных белков, что приводит к повышению проницаемости биологических мембран. Кроме того, накопление лактата в мышечных клетках ведёт к набуханию этих клеток вследствия поступления в них воды, что в итоге уменьшает сократительные возможности мышц. Можно также предположить, что избыток лактата внутри миоцитов связывает часть ионов кальция и тем самым ухудшает управление процессами сокращения и расслабления, что особенно сказывается на скоростных свойствах мышцы.
Известные в настоящее время биохимические методы оценки использования при физической работе гликолитического пути ресинтеза АТФ основаны на оценке биохимических сдвигов в организме, обусловленных накоплением молочной кислоты. Одним из показателей, отражающих накопление в кровяном русле молочной кислоты, является водородный показатель крови (рН). В покое этот показатель равен 7,36 – 7,40, а после интенсивной работы он снижается до 7,2 – 7,0.
Ещё один метод оценки скорости гликолиза, фиксирующий последствия образования и накопления молочной кислоты – это определение щелочного резерва крови. Щелочной резерв крови – это щелочные компоненты всех буферных систем крови. При поступлении во время мышечной работы в кровь молочной кислоты она вначале нейтрализуется путём взаимодействия с буферными системами крови, и поэтому происходит снижение щелочного резерва крови.
Также может быть использовано определение лактатного кислородного долга. Лактатный кислородный долг – это повышенное потребление кислорода в ближайшие 1 – 1,5 часа после окончания мышечной работы. Этот избыток кислорода необходим для устранения молочной кислоты, образовавшейся при работе. Наибольшие величины лактатного кислородного долга определяются после физических нагрузок продолжительностью 2 – 3 минуты, выполняемых с предельной интенсивностью. У хорошо тренированных спортсменов величина лактатного кислородного долга может достигать 20 л.
Самым основным методом оценки гликолитического пути образования АТФ является определение после физической нагрузки концентрации лактата в крови.
Аэробный (при участии кислорода) ресинтез – основной путь новообразования АТФ в организме. Кислород, поступающий в организм в процессе дыхания, выступает в роли акцептора водорода (протонов и электронов), отщепляемого в ходе биологического окисления от окисляемых веществ. Энергия, освобождающаяся в процессе переноса водорода (электронов) от окисляемого вещества на кислород, частично (до 60%) используется на ресинтез АТФ, частично освобождается в виде тепла.
Характеристика возможностей аэробного окисления дана ранее. Как уже отмечалось, аэробный ресинтез отличается высокой эффективностью. Однако эффективность аэробного процесса не является постоянной величиной и может варьировать. Эти вариации эффективности вызываются изменениями степени сопряжения окисления с фосфорилированием (ресинтезом АТФ) в процессе переноса электронов от окисляемого субстрата на кислород. В этом случае уменьшается доля энергии, используемая на ресинтез АТФ, и увеличивается освобождение энергии в виде тепла. Частичное разобщение окисления с ресинтезом АТФ наблюдается в тех случаях, когда энергетические обеспечение работы осуществляется за счет интенсивно идущих аэробных и анаэробных процессов (гликолиза), при утомлении, вызванном мышечной работой. Непосредственной причиной снижения эффективности аэробных процессов в этих условиях является накопление высоких концентраций продуктов обмена.
Скорость образования АТФ при этом может не снижаться и даже возрастать. Но из-за снижения эффективности аэробных превращений увеличивается скорость расходования энергетических ресурсов организма. Кроме того, для ресинтеза того же количества АТФ требуется больше кислорода и энергетических субстратов. Это, в свою очередь, требует более напряженной работы систем доставки и утилизации кислорода, в первую очередь, дыхательной и сердечно-сосудистой.
Значительное преимущество перед анаэробными процессами аэробный путь ресинтеза имеет по метаболической емкости. Емкость аэробных превращений можно рассматривать как практически безграничную. Аэробные процессы обеспечивают организм энергией с первых до последних мгновений жизни, не прерываясь ни на минуту. Однако для спортивной практики интерес представляет не способность аэробного процесса функционировать непрерывно на протяжении всей жизни человека, а возможность поддерживать высокую интенсивность его деятельности. В научных исследованиях в качестве показателя метаболической емкости аэробного процесса используется время удержания максимального кислородного потребления (МПК) или какого либо процента от этого уровня. У нетренированных лиц время удержания МПК составляет 7-9 мин, у квалифицированных спортсменов, специализирующихся в «аэробных» видах спорта (легкоатлетический бег на длинные дистанции, лыжные гонки и т.п.), время удержания этого показателя может достигать 30 и более минут. При снижении интенсивности работы и, следовательно, уровня потребления кислорода, время удержания этого уровня и, следовательно, время работы увеличиваются.
В таблице 8 представлены данные, характеризующие возможности основных биохимических механизмов преобразования энергии.
Таблица 8.
Характеристика важнейших механизмов энергетического обеспечения мышечной работы
Среди факторов, определяющих скорость аэробных превращений при мышечной работе, можно выделить следующие основные:
· Потребность в энергии (скорость расщепления АТФ).
· Скорость поставки кислорода к работающим мышцам и другим органам и тканям.
· Доступность субстратов окисления.
· Активность ферментных систем аэробного окисления (рис. 64).
Рис. 64. Факторы, определяющие скорость аэробных превращений при работе
В обычных условиях потребность в энергии является основным фактором, регулирующим скорость аэробных превращений. Непосредственным регулятором является соотношение концентраций АТФ, АДФ и неорганического фосфата (Н 3 РО 4). При этом ведущую роль в изменении скорости аэробного процесса играет изменение концентрации АДФ. Зависимость скорости аэробного процесса от концентрации АДФ получило название «дыхательного контроля».
В покоящейся мышце числовое значение отношения [АТФ] / [АДФ] достаточно велико и скорость аэробных превращений невысокая. С началом мышечной работы отношение [АТФ] / [АДФ] резко уменьшается как за счет уменьшения концентрации АТФ, так и за счет увеличения концентрации АДФ и скорость аэробных превращений возрастает.
В экспериментах на препаратах мышечной ткани, содержащей компоненты дыхательной цепи, субстраты окисления и кислород, установлено, что добавление в такую смесь даже небольших количеств АДФ мгновенно увеличивает скорость аэробных превращений практически до максимума. Однако, в организме человека при напряженной мышечной работе и высокой концентрации АДФ в качестве фактора, определяющего скорость аэробных превращений, кроме концентрации АДФ, выступает скорость поставки кислорода, которая нередко становится главным лимитирующим фактором.
Потребление кислорода и его транспорт к работающим мышцам и другим органам и тканям осуществляется при участи многих органов и систем организма и зависит в первую очередь от:
· возможностей аппарата внешнего дыхания;
· диффузионной способности легких;
· кислородной емкости крови, зависящей от содержания гемоглобина в крови и его сродства к кислороду;
· сердечной производительности, связанной с размерами левого желудочка, силой сердечной мышцы и частотой сердечных сокращений;
· условий кровоснабжения работающих мышц и органов: их капилляризации, просвета периферических капилляров, их тонуса при работе;
Многочисленные научные данные свидетельствуют о том, что наиболее значимыми для снабжения тканей кислородом из перечисленных факторов, являются кислородная емкость крови, сердечная производительность и кровоснабжение работающих мышц.
Как уже указывалось, одним из факторов, ограничивающих мощность (и особенно) емкость аэробного ресинтеза АТФ, может быть доступность субстратов окисления. Наиболее заметно это может проявляться при продолжительной мышечной работе. На начальных этапах такой работы в качестве энергетического субстрата используется преимущественно гликоген мышц. Запасы гликогена в мышечной ткани заметно повышаются под влиянием систематической тренировки и у хорошо тренированных спортсменов, специализирующихся в видах спорта с продолжительными нагрузками, могут увеличиваться в два и более раз по сравнению с нетренированными и достигать 3% и более от массы мышечной ткани. Это, однако, не решает проблемы обеспечения продолжительной работы энергетическими субстратами.
По мере истощения внутримышечных углеводных ресурсов источником энергии для мышц (и других тканей) может стать гликоген печени. Мобилизация гликогена печени происходит под влиянием гормонов адреналина, норадреналина, глюкагона. Однако, использование мышцами выходящей из печени в кровь глюкозы возможно только при достаточно высокой концентрации инсулина в крови. Это, в свою очередь, возможно только при повышенном содержании в крови глюкозы, что маловероятно в условиях длительной работы.
Следующий важнейший энергетический субстрат при мышечной работе – жиры. Запасы жиров имеются в мышечных клетках (как и в клетках других органов и тканей) и в так называемых жировых депо организма: подкожной жировой ткани, сальниках, брыжейках. Внутримышечные жиры используются в самих мышечных волокнах. Их мобилизация начинается при снижении содержания мышечного гликогена.
Мобилизация жира из депо (липолиз) происходит при снижении содержания глюкозы в крови, которое сопровождается также снижением в крови инсулина. Пониженное содержание глюкозы в крови является ведущим фактором, обеспечивающим мобилизацию жира из депо.
Уменьшение концентрации инсулина в крови затрудняет диффузию глюкозы через мембраны мышечных клеток и ограничивает ее использование мышцами в качестве источника энергии. В этих условиях глюкоза крови утилизируется преимущественно мозгом и нервными волокнами, а также сердцем, оболочки которых не чувствительны к инсулину.
Липолитическим действием обладают гормоны симпатоадреналовой системы (адреналин, норадреналин), а также соматотропин, кортикотропин, тиреотропин, лютеотропин, кортикостероиды, секретин.
Образующиеся в процессе мобилизации жиров глицерин и жирные кислоты выходят в кровь. Глицерин извлекается из крови печенью, где из него синтезируется глюкоза. Глюкоза выходит из печени в кровь и используется различными тканями (в условиях мобилизации жиров из депо и низкого содержания инсулина в крови преимущественно мозгом и нервными волокнами) в качестве энергетического субстрата.
Использование жирных кислот крови может происходить двумя путями. Во-первых, они утилизируются мышечными и некоторыми другими клетками, где окисляются в аэробных превращениях до СО 2 и Н 2 О. Значительная часть жирных кислот задерживается печенью, где происходит их превращение в кетоновые тела: ацетоуксусную кислоту и бета-гидроксибутират. Кетоновые тела - низкомолекулярные соединения, обладающие хорошей растворимостью в воде и высокой диффузионной способностью. Они поступают из печени в кровоток и утилизируются практически всеми активно функционирующими тканями, где используются в качестве источника энергии в аэробных превращениях.
Таким образом, печень выполняет своеобразную вспомогательную функцию при использовании депонированных жиров в качестве источника энергии.
Наряду с углеводами и жирами в условиях длительной мышечной работы в качестве источника энергии могут использоваться и продукты превращений белков – аминокислоты. Непрерывно происходящий процесс распада белков при выполнении мышечной работы может усиливаться. В первую очередь это относится к белкам, выполняющим какую либо работу: сократительным, ферментам и т.п. В тоже время процессы синтеза белка во время мышечной работы приостанавливаются главным образом из-за дефицита энергии. Результатом этой диспропорции процессов распада и синтеза белков является выход в кровь свободных аминокислот. Аминокислоты крови во время мышечной работы утилизируются преимущественно печенью. Часть этих аминокислот подвергается дезаминированию и включается в процессы глюконеогенеза (синтеза глюкозы). Таким образом, при продолжительной мышечной работе аминокислоты могут служить еще одним энергетическим субстратом, превращаясь в наиболее дефицитные в этих условиях вещества – углеводы.
Бесперебойное обеспечение работающих мышц и других органов и тканей энергетическими субстратами зависит не только от их общих запасов в организме. Важную роль играет их мобилизация, транспорт, диффузия к местам использования, предварительная переработка ряда субстратов. Эти процессы совершаются при участии многих желез внутренней секреции, в первую очередь, надпочечников, поджелудочной железы, гипофиза, а также симпатической нервной системы, деятельность которых должна быть строго скоординирована. Снижение продукции соответствующих гормонов вследствие истощения желез внутренней секреции, или по другим причинам, нарушение координации в их деятельности может оказать серьезное влияние на обеспечение энергетического обмена субстратами.